Современная химия – это сложный многогранный предмет изучения, благодаря которому можно изучить все аспекты и особенности устройства мира на атомном уровне. Все живое является определенным сочетанием атомов в химических связях. Выделяют три их вида:
- Металлическая. В ней электроны атомов свободны.
- Ионная. Один из атомов отдает свои электроны другому элементу.
- Ковалентная. Представляет собой разновидность химической связи, при которой у обоих атомов, находящихся в реакции, появляются совместные электроны.
 Электронные пары, образованные в ковалентной связи размещаются на внешних подуровнях электронов. Различают два вида самой связи: полярная и неполярная ковалентная связь, и них есть существенное различие. В неполярной связи всегда атомы одного и того же вещества. А в полярной – разных.
Электронные пары, образованные в ковалентной связи размещаются на внешних подуровнях электронов. Различают два вида самой связи: полярная и неполярная ковалентная связь, и них есть существенное различие. В неполярной связи всегда атомы одного и того же вещества. А в полярной – разных.
Валентность химического вещества – это его способность образовывать определенное количество химических связей. Если речь идет о ковалентной полярной связи, то валентность химического элемента определяется числом образованных в результате реакции двухэлектронных связей. Такой подход был сформулирован в теории локализованных валентных связей, выдвинутой в начале двадцатого века.
Ковалентность элемента – это общее число неспаренных электронов, то есть способность химического элемента образовать ковалентную связь.
По валентности элементов составляются истинные формулы и наоборот. Главное придерживаться следующего принципа: произведение валентности первого элемента на число его атомов равно произведению валентности второго элемента на число его атомов.
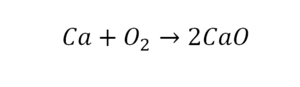 Уравнение химической реакции – это запись химического процесса в виде формулы с использованием математических знаков. В первую очередь важно разобраться с кем, как ставить коэффициенты в химических уравнениях – методом подстановки. Коэффициент – это та цифра, которая ставится перед элементом или уравнением в целом. Вне зависимости от того, где конкретно стоит коэффициент, он окажет влияние на все последующие элементы в формуле.
Уравнение химической реакции – это запись химического процесса в виде формулы с использованием математических знаков. В первую очередь важно разобраться с кем, как ставить коэффициенты в химических уравнениях – методом подстановки. Коэффициент – это та цифра, которая ставится перед элементом или уравнением в целом. Вне зависимости от того, где конкретно стоит коэффициент, он окажет влияние на все последующие элементы в формуле.
Правила расстановки коэффициентов в химической реакции:
- Коэффициент относится ко всем символам и умножается на индекс (число за элементом) каждого символа.
- Количество атомов, вступающих в реакцию должно совпадать с количеством атомов в результате процесса.
При проведении химических реакций важно помнить про правила безопасности. Предварительно важно просчитать все на бумаге и при получении неизвестной формулы – уточнить у специалиста или в учебных материалах, какой будет результат, перед тем как применять на практике.
 Женский журнал издание для женщин
Женский журнал издание для женщин